1. Đại cương
Hen phế quản là một bệnh lý viêm mạn tính của đường thở, đặc trưng bởi tình trạng viêm dai dẳng, tăng đáp ứng phế quản và tắc nghẽn luồng khí biến đổi theo thời gian. Trên toàn cầu, hen ảnh hưởng đến hơn 300 triệu người và tiếp tục gia tăng, đặc biệt tại các quốc gia có thu nhập trung bình và thấp [1]. Mặc dù đa số bệnh nhân có thể kiểm soát tốt triệu chứng bằng điều trị chuẩn, khoảng 5–10% bệnh nhân thuộc nhóm hen nặng, nhưng nhóm này lại chiếm phần lớn gánh nặng về chi phí y tế, nhập viện và tử vong liên quan đến hen [1].
Hen nặng được định nghĩa là hen vẫn không kiểm soát được dù đã điều trị tối ưu bằng corticosteroid dạng hít liều cao phối hợp với ít nhất một thuốc kiểm soát khác, hoặc cần corticosteroid đường toàn thân để duy trì kiểm soát bệnh [2]. Cần phân biệt hen nặng với hen khó điều trị, trong đó kiểm soát kém chủ yếu do các yếu tố có thể điều chỉnh như tuân thủ điều trị kém, kỹ thuật dùng thuốc không đúng hoặc bệnh đồng mắc chưa được xử trí đầy đủ [1].
Nhiều yếu tố góp phần vào tình trạng kém đáp ứng điều trị ở bệnh nhân hen nặng, bao gồm sự tồn tại đồng thời nhiều kiểu hình viêm, tái cấu trúc đường thở tiến triển và các bệnh đồng mắc như viêm mũi xoang mạn, polyp mũi, béo phì và trào ngược dạ dày–thực quản [3]. Những hạn chế của liệu pháp truyền thống, đặc biệt là corticosteroid đường toàn thân với nhiều tác dụng không mong muốn nghiêm trọng, đã thúc đẩy sự phát triển của các liệu pháp sinh học nhắm trúng đích trong điều trị hen nặng [2].
2. Cơ chế bệnh sinh của hen nặng
2.1. Hen nặng có cơ chế bệnh sinh phức tạp với nhiều kiểu hình viêm
Hen nặng là một phân nhóm nhỏ của hen với nhiều kiểu hình và cơ chế bệnh sinh khác nhau. Dựa trên đặc điểm viêm, hen thường được phân thành hai nhóm lớn: viêm typ 2 (type 2-high) và viêm không typ 2 (type 2-low) [4]. Viêm typ 2 chiếm khoảng một nửa số bệnh nhân hen và là cơ sở sinh học của phần lớn các liệu pháp sinh học hiện nay [4].
Hình 19.1. Sinh bệnh học phức tạp của hen nặng (nguồn: Lancet 2023)
Viêm typ 2 được trung gian chủ yếu bởi các cytokine IL-4, IL-5 và IL-13, do tế bào lympho T hỗ trợ typ 2 (Th2) và các tế bào lympho bẩm sinh typ 2 (ILC2) tiết ra. Các cytokine này thúc đẩy tăng sinh và hoạt hóa bạch cầu ái toan, chuyển lớp kháng thể IgE, tăng tiết nhầy và co thắt cơ trơn phế quản, dẫn đến triệu chứng lâm sàng và đợt kịch phát hen [4,5].
Ngược lại, hen không typ 2 thường đặc trưng bởi viêm bạch cầu trung tính hoặc viêm nghèo tế bào, ít đáp ứng với corticosteroid và hiện vẫn thiếu các liệu pháp nhắm trúng đích hiệu quả [5].
2.2. Vai trò trung tâm của viêm typ 2 và sự nổi lên của TSLP
Trong những năm gần đây, nhận thức về vai trò của biểu mô đường thở trong sinh bệnh học hen đã thay đổi đáng kể. Biểu mô không chỉ là hàng rào cơ học mà còn là nguồn tiết các cytokine khi bị tổn thương bởi dị nguyên, virus hô hấp, ô nhiễm không khí hoặc khói thuốc lá [4].
Trong số các cytokin viêm, thymic stromal lymphopoietin (TSLP) trong những năm gần đẩy nổi lên như một nhân tố then chốt, đóng vai trò khởi phát và khuếch đại phản ứng viêm trong hen nặng. TSLP thúc đẩy hoạt hóa tế bào tua gai, cảm ứng biệt hóa Th2, đồng thời kích thích ILC2, dưỡng bào, bạch cầu ái toan và bạch cầu ưa bazơ tiết các cytokine typ 2 [6]. Đáng chú ý, TSLP không chỉ liên quan đến hen typ 2 mà còn góp phần vào tăng đáp ứng phế quản và tái cấu trúc đường thở trong hen không typ 2 [6].
Ở mức độ phân tử, TSLP phát huy tác dụng thông qua phức hợp thụ thể gồm TSLPR (CRLF2) và chuỗi α của thụ thể IL-7 (IL-7Rα). Sự hình thành phức hợp TSLP–TSLPR–IL-7Rα là điều kiện cần thiết để kích hoạt các đường truyền tín hiệu nội bào liên quan đến viêm [7]. Từ TSLP, phản ứng viêm được dẫn truyền qua ba con đường chính: con đường dị ứng qua hoạt hóa Th2 và sản xuất IgE; con đường viêm eosinophil qua ILC2 và IL-5; và con đường vượt ngoài typ 2 thông qua Th17, bạch cầu trung tính và tế bào cấu trúc đường thở như hình 19.2.
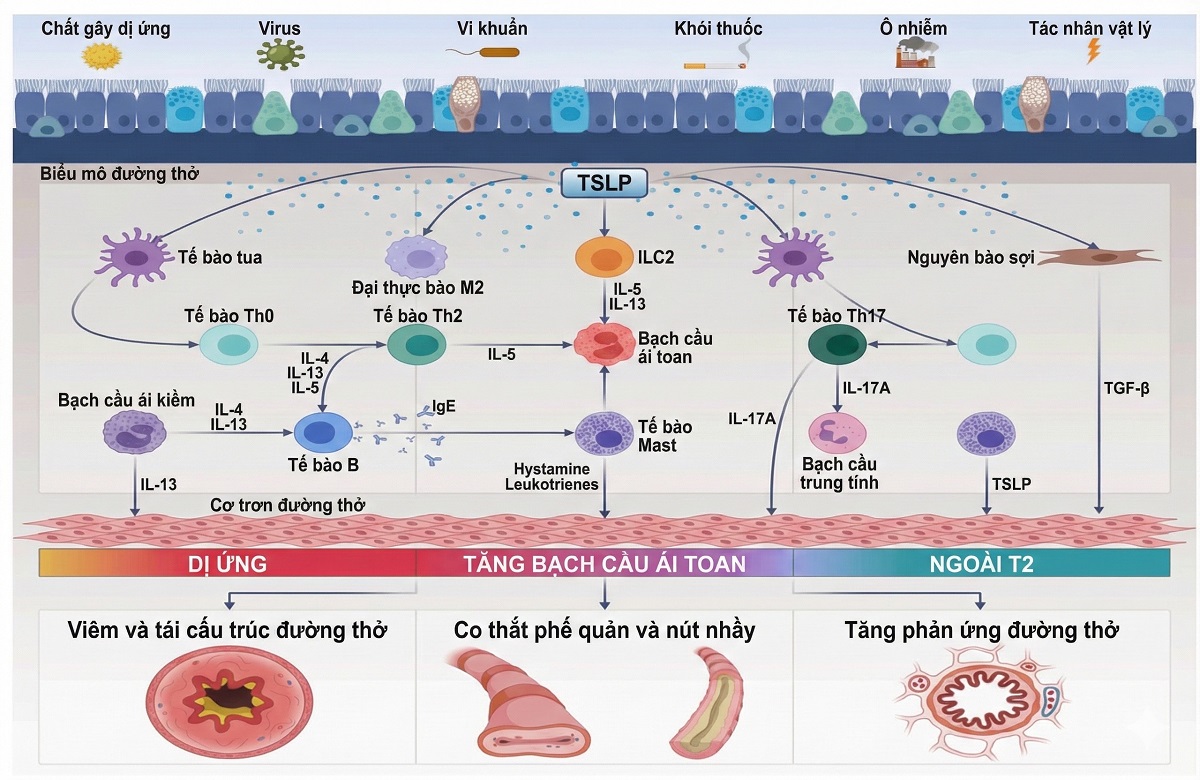
Hình 19.2. Vai trò và vị trí của TSLP trong cơ chế viêm của hen dị ứng
(nguồn: Pelaia C et al (2025) Front. Allergy 6:1671353.)
3. Dược lý lâm sàng của thuốc sinh học trong điều trị hen nặng
3.1. Dược lý phân tử của các kháng thể đơn dòng trong điều trị hen nặng
Liệu pháp sinh học trong hen nặng bao gồm các kháng thể đơn dòng nhắm trúng các phân tử then chốt trong con đường viêm typ 2, như IgE, IL-5, thụ thể IL-5, IL-4Rα và TSLP [2,5].
Trước khi xuất hiện các liệu pháp nhắm trúng đích thượng nguồn, các thuốc sinh học trong điều trị hen nặng chủ yếu tập trung vào các mắt xích hạ nguồn của viêm typ 2. Omalizumab ức chế IgE tự do, trong khi mepolizumab, reslizumab và benralizumab tác động lên trục IL-5 nhằm làm giảm số lượng và hoạt tính bạch cầu ái toan. Dupilumab ức chế tín hiệu IL-4/IL-13 thông qua thụ thể IL-4Rα, từ đó làm giảm viêm, tăng tiết nhầy và tái cấu trúc đường thở [2,5].
Bảng 19.1. Các thuốc sinh học (kháng thể đơn dòng) trong điều trị hen nặng
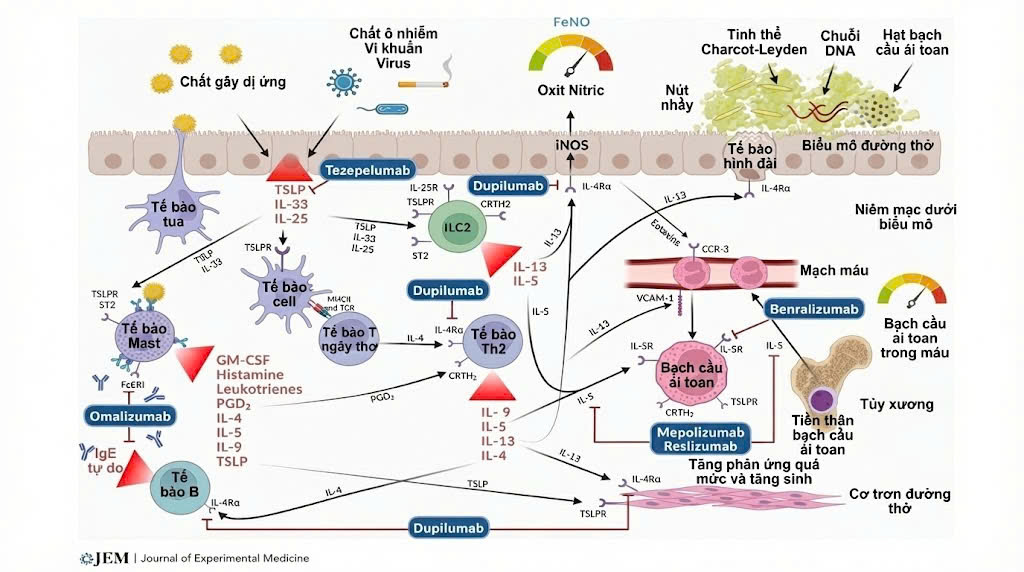
Cho đến nay, tezepelumab là kháng thể đơn dòng đầu tiên nhắm trực tiếp vào TSLP và đại diện cho chiến lược điều trị mới nhắm vào yếu tố thượng nguồn của phản ứng viêm như hình 19.3. Khác với các thuốc sinh học khác tác động chủ yếu lên các cytokine hạ nguồn, tezepelumab ức chế TSLP tự do, ngăn không cho cytokine này gắn với phức hợp thụ thể TSLPR/IL-7Rα [7].
Các nghiên cứu cấu trúc đã làm sáng tỏ cơ chế phân tử của quá trình này. TSLP trước tiên gắn với TSLPR, gây ra thay đổi cấu dạng giúp tuyển mộ IL-7Rα để hình thành phức hợp tín hiệu hoàn chỉnh. Tezepelumab gắn vào bề mặt TSLP theo cách làm gián đoạn quá trình viêm này ngay từ đầu, từ đó ngăn chặn sự hình thành phức hợp thụ thể và toàn bộ chuỗi tín hiệu viêm phía sau [7]. Cơ chế này giải thích khả năng ức chế rộng của tezepelumab đối với cả viêm typ 2 và một phần viêm không typ 2.
Hình 19.3. Cơ chế tác dụng của các thuốc sinh học trên con đường viêm typ2
(Nguồn: Howell I et al. J Exp Med. 2023;220(7):e20221212.)
3.2. Bằng chứng hiệu quả lâm sàng
Các liệu pháp sinh học kinh điển như omalizumab, mepolizumab, benralizumab và dupilumab cũng đã chứng minh hiệu quả lâm sàng rõ rệt trong việc giảm đợt kịch phát, cải thiện kiểm soát triệu chứng và chức năng hô hấp ở các phân nhóm hen nặng phù hợp với kiểu hình viêm typ 2. Hiệu quả của các thuốc này phụ thuộc chặt chẽ vào đặc điểm sinh học nền như IgE, bạch cầu ái toan và FeNO, nhấn mạnh vai trò của tiếp cận điều trị cá thể hóa [2,5].
Điểm nổi bật của tezepelumab qua thử nghiệm pha III NAVIGATOR là khả năng làm giảm đáng kể tần suất đợt kịch phát hen và cải thiện chức năng hô hấp so với giả dược, bao gồm FEV₁ trước và sau giãn phế quản, với sự duy trì bền vững trong suốt 52 tuần và đồng thời tác động lên nhiều thông số phổi, bao gồm cả đường thở nhỏ. [8]. Hiệu quả này được ghi nhận tezepelumab với mức bạch cầu ái toan ban đầu, cho thấy phạm vi tác động rộng hơn so với nhiều thuốc sinh học khác [8].
Theo GINA 2025, liệu pháp sinh học được khuyến cáo là một phần quan trọng trong kiểm soát hen ở những bệnh nhân hen nặng hay hen bậc 5 [11].
3.3. Bằng chứng về an toàn thuốc trong điều trị
Nhìn chung, các thuốc sinh học trong điều trị hen nặng có hồ sơ an toàn thuận lợi. Phân tích dữ liệu cảnh giác dược toàn cầu cho thấy các tác dụng không mong muốn thường gặp bao gồm phản ứng tại chỗ tiêm, viêm mũi họng, đau đầu và mệt mỏi [9]. Một số tín hiệu an toàn hiếm gặp đã được ghi nhận, tuy nhiên cần thêm nghiên cứu để xác định mối liên quan nhân quả và ý nghĩa lâm sàng lâu dài [9]. Về tương tác thuốc, các dữ liệu hiện có cho thấy bản thân thuốc sinh học hầu như không tham gia tương tác dược động học đáng kể. Nguy cơ tương tác chủ yếu xuất phát từ tình trạng đa trị liệu ở bệnh nhân hen nặng, đặc biệt với corticosteroid đường toàn thân, thuốc giãn phế quản, bao gồm chủ vận β2 và kháng cholinergic, và các thuốc điều trị bệnh đồng mắc [10].
4. Triển vọng ứng dụng thuốc sinh học trong điều trị hen nặng
Liệu pháp sinh học đã làm thay đổi căn bản cách tiếp cận điều trị hen nặng, cho phép điều trị cá thể hóa dựa trên cơ chế bệnh sinh và biomarker. Các lợi ích chính bao gồm giảm đợt kịch phát, giảm phụ thuộc corticosteroid đường toàn thân và cải thiện chất lượng cuộc sống [2,5].
Tuy nhiên, việc lựa chọn thuốc sinh học phù hợp vẫn là thách thức, do thiếu các biomarker dự đoán đáp ứng chính xác cho từng bệnh nhân, đặc biệt trong hen không typ 2. Do đó, các hướng dẫn hiện nay nhấn mạnh vai trò của mô hình quản lý đa chuyên khoa, với sự phối hợp giữa bác sĩ hô hấp, dị ứng, tai mũi họng và dược sĩ lâm sàng nhằm tối ưu hóa hiệu quả và an toàn điều trị [1,3].
Về mặt chi phí–hiệu quả, các phân tích kinh tế y tế cho thấy thuốc sinh học giúp giảm đợt kịch phát và cải thiện chất lượng cuộc sống nhưng hiện vẫn có chi phí cao, với tỷ lệ chi phí trên mỗi năm sống điều chỉnh theo chất lượng còn vượt ngưỡng chấp nhận thông thường. Do đó, việc lựa chọn đúng bệnh nhân và tối ưu hóa sử dụng thuốc có ý nghĩa then chốt để nâng cao giá trị điều trị [12].
5. Kết luận
Hen nặng là một bệnh lý phức tạp, đòi hỏi cách tiếp cận điều trị dựa trên hiểu biết sâu sắc về cơ chế bệnh sinh. Sự tiến bộ trong sinh học miễn dịch, đặc biệt là vai trò trung tâm của TSLP như một yếu tố khởi phát thượng nguồn, đã mở ra kỷ nguyên của các liệu pháp sinh học nhắm trúng đích. Trong đó, tezepelumab đại diện cho một bước tiến quan trọng với cơ chế tác động rộng và hiệu quả lâm sàng đã được chứng minh. Trong tương lai, các tiến bộ về sinh học và dược lý phân tử cũng như mô hình chăm sóc đa chuyên khoa sẽ đóng vai trò then chốt trong tối ưu hóa điều trị hen nặng.
Tài liệu tham khảo
1. Faria N, Costa MI, Fernandes AL, et al. Biologic Therapies for Severe Asthma: Current Insights and Future Directions. J Clin Med. 2025.
2. Gyawali B, Georas SN, Khurana S. Biologics in severe asthma: a state-of-the-art review. Eur Respir Rev. 2025.
3. Treatment of Severe Asthma Is Not “Cookie-Cutter” Medicine. Am J Respir Crit Care Med.
4. Howell I, Howell A, Pavord ID. Type 2 inflammation and biological therapies in asthma. J Exp Med. 2023.
5. Vărut RM, Dalia D, Radivojevic K, et al. Targeted Biologic Therapies in Severe Asthma. Pharmaceuticals. 2025.
6. Pelaia C, et al. Key role of thymic stromal lymphopoietin as a molecular target for biologic treatment of severe asthma. Front Allergy. 2025.
7. Verstraete K, et al. Structure and antagonism of the receptor complex mediated by human TSLP. Nat Commun. 2017.
8. Menzies-Gow A, et al. Effect of Tezepelumab on Lung Function in Severe Asthma (NAVIGATOR). Adv Ther. 2023.
9. Cutroneo PM, et al. Safety of Biological Therapies for Severe Asthma. BioDrugs. 2024.
10. Momcilovic et al (2025). A retrospective study on potential drug‒drug interactions in patients with severe asthma receiving biological therapy: a single-center experience. BMC pulmonary medicine, 25(1), 23.
11. Venkatesan P. 2025 GINA report for asthma. Lancet Respir Med. Published online June 26, 2025.
12. Tice, J. A et al (2019). The Effectiveness and Value of Biologic Therapies for the Treatment of Uncontrolled Asthma. Journal of managed care & specialty pharmacy, 25(5), 510–514.
ThS.DS.Nguyễn Thiên Vũ
DSCKI.Huỳnh Ngọc Hoàn Mỹ
Đơn vị DLS-TTT, Khoa Dược Bệnh viện Trường ĐHYD Cần Thơ