1.3 Vai trò của việc quản lý sử dụng albumin trên thực hành lâm sàng
Trong sản xuất, HSA được chiết, tách từ huyết tương người khỏe mạnh, dẫn đến sự khan hiếm nguồn cung và giá thành cao, tạo ra gánh nặng trong thực hành, đòi hỏi việc sử dụng albumin cần có chiến lược quản lý phù hợp và ưu tiên cho những chỉ định thật sự có lợi ích lâm sàng [5].
Thực tế, albumin truyền tĩnh mạch có khuynh hướng sử dụng quá mức cho những chỉ định thiếu chứng cứ hoặc không được khuyến cáo [18]. Các đồng thuận hiện nay không khuyến cáo sử dụng albumin để cải thiện dinh dưỡng và thúc đẩy tốc độ hồi phục sau phẫu thuật [5]. Quản lý albumin trong thực hành không chỉ giúp giảm áp lực nguồn cung hạn chế mà còn giúp giảm chi phí điều trị, bao gồm chi phí cho các quỹ bảo hiểm y tế [5], [14]. Không những vậy, việc hạn chế sử dụng albumin với những chỉ định không phù hợp còn giúp hạn chế các biến cố bất lợi liên quan đến thuốc như gây quá tải dịch, phản ứng phản vệ, tăng số lượng hồng cầu và hoại tử ngoại biên [18].
2. Các khuyến cáo sử dụng albumin đường tĩnh mạch [14]
Bảng 3.2. Cập nhật khuyến cáo liên quan đến truyền albumin người trong thực hành
.jpg)
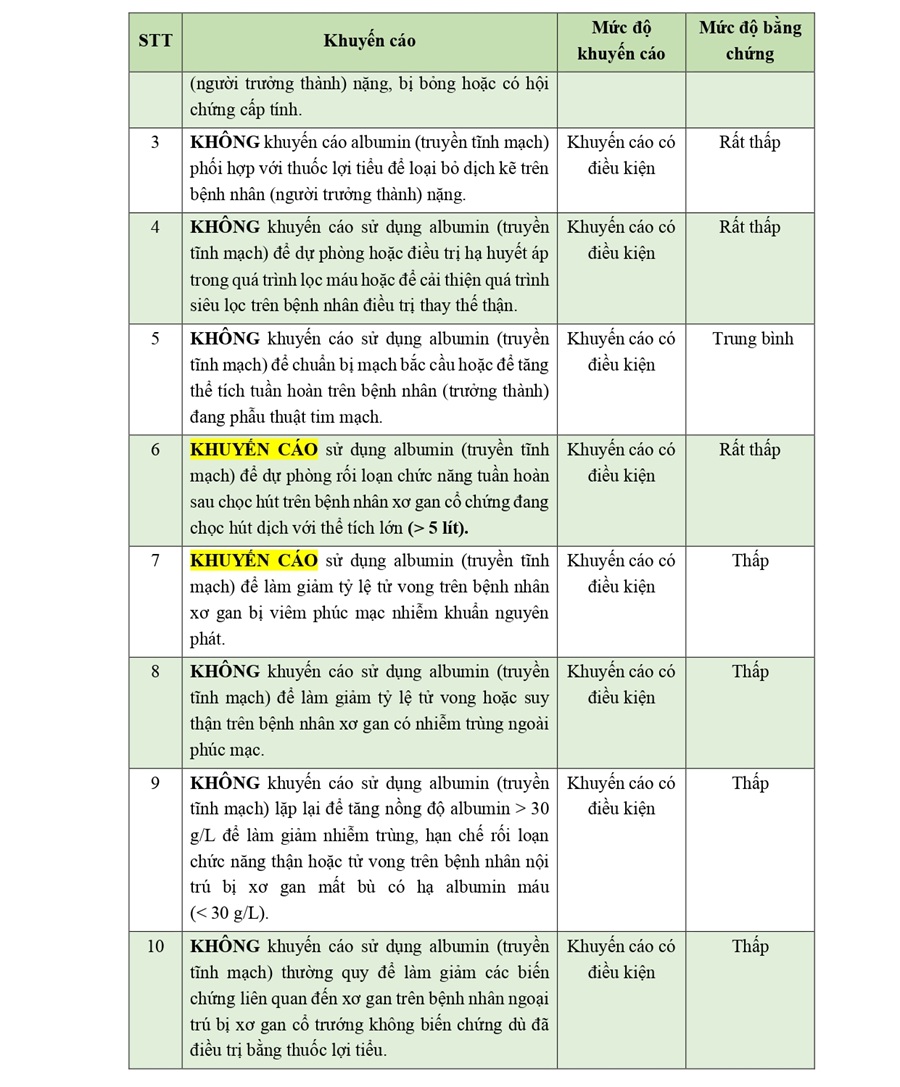
* Lưu ý: Các trường hợp albumin có khuyến cáo chỉ định phải thỏa mãn điều kiện nồng độ albumin huyết thanh < 25g/L hoặc trong tình trạng sốc , hoặc có hội chứng suy hô hấp cấp tiến triển [2], [3], [4].
3. Chỉ định không phù hợp [16]
Bảng 3.3. Một số chỉ định không phụ hợp về truyền albumin trong thực hành
.jpg)
5. Một số lưu ý khi sử dụng albumin trên lâm sàng lâm sàng
5.1 Một số vấn đề về pha, tiêm truyền khi sử dụng albumin [1]
- Tốc độ truyền khuyến cáo cho bệnh nhân người lớn ở thể trạng bình thường là 1mL/phút, thời gian truyền 1 chai < 4 giờ;
- Các chế phẩm albumin 5% là dung dịch đẳng trương, chế phẩm albumin 20% hay 25% là dung dịch ưu trương, chỉ dùng trong truyền tĩnh mạch;
- Trường hợp cần pha loãng dung dịch albumin ưu trương (20%, 25%), dung môi phù hợp là dung dịch NaCl 0,9%, dung dịch Dextrose 5% hay dung dịch Glucose 5%;
- Không pha loãng dung dịch albumin bằng nước cất do có khả năng gây tan máu;
- Không sử dụng nếu lọ đã mở nắp sau 4 giờ.
5.2 Chống chỉ định và thận trọng [1]
- Chống chỉ định: bệnh nhân thiếu máu nặng hoặc suy tim với thể tích máu nội mạch bình thường hoặc tăng.
- Phản ứng có hại thường gặp nhất sau khi truyền: sốt và ớn lạnh; nổi mẫn, buồn nôn, nôn, nhịp tim nhanh…
- Một số biến cố bất lợi khác cần thận trọng:
+ Tốc độ truyền quá nhanh hơn khuyến cáo có thể gây tình trạng phù phổi;
+ Huyết áp tăng nhanh sau khi truyền cần được theo dõi chặt chẽ ở những bệnh nhân có chấn thương hoặc hậu phẫu.
Điều kiện thanh toán Bảo hiểm Y tế đối với albumin truyền tĩnh mạch [3], [4]
* Lưu ý: Theo thông tư 20/2022/TT- BYT, chỉ định truyền albumin được Quỹ bảo hiểm y tế thanh toán 70% trong các trường hợp: Nồng độ albumin < 25g/L hoặc sốc hoặc hội chứng suy hô hấp tiến triển.
TÀI LIỆU THAM KHẢO
1. Thông tin kê toa của nhà sản xuất đi kèm với chế phẩm Albuterin 25%
2. Bộ Y tế (2015), Hướng dẫn chẩn đoán và xử trí Hồi sức tích cực.
3. Thông tư 20/2022/TT-BYT ban hành Danh mục và tỷ lệ, điều kiện thanh toán đối với thuốc hóa dược, sinh phẩm, thuốc phóng xạ và chất đánh dấu thuộc phạm vi được hưởng của người tham gia bảo hiểm y tế.
4. Thông tư 37/2024/TT-BYT quy định nguyên tắc, tiêu chí xây dựng, cập nhật, ghi thông tin, cấu trúc danh mục và hướng dẫn thanh toán đối với thuốc hóa dược, sinh phẩm, thuốc phóng xạ và chất đánh dấu thuộc phạm vi được hưởng của người tham gia bảo hiểm y tế.
5. Huang X, Jiang X, Xiong F, Fu X, Hong L, Xu X, Lin Z. Rational use of human albumin: plan-do-check-act cycle in clinical practice. BMJ Support Palliat Care. 2025 Jan 20:spcare-2024-005268.
6.Fanali G, di Masi A, Trezza V, Marino M, Fasano M, Ascenzi P. Human serum albumin: from bench to bedside. Mol Aspects Med 2012;33:209–90.
7.Hubner M, Mantziari S, Demartines N, Pralong F, Coti-Bertrand P, Schafer M. Postoperative albumin drop is a marker for surgical stress and a predictor for clinical outcome: a pilot study. Gastroenterol Res Pract. 2016;2016:8743187.
8. Kaysen GA, Dubin JA, Muller HG, et al. Inflammation and reduced albumin synthesis associated with stable decline in serum albumin in hemodialysis patients. Kidney Int. 2004;65(4):1408-1415.
9. Fleck A, Raines G, Hawker F, et al. Increased vascular permeability: a major cause of hypoalbuminaemia in disease and injury. Lancet. 1985;1(8432):781-784.
10. Allison SP, Lobo DN. The clinical significance of hypoalbuminaemia. Clin Nutr. 2024 Apr;43(4):909-914.
11. Horowitz IN, Tai K. Hypoalbuminemia in critically ill children. Arch Pediatr Adolesc Med. 2007;161(11):1048-1052.
12. Chappell D, Jacob M, Hofmann-Kiefer K, Conzen P, Rehm M. A rational approach to perioperative fluid management. Anesthesiology. 2008;109(4):723-740.
13. Abdelhamid S, Achermann R, Hollinger A, Hauser M, Trutmann M, Gallacchi L, Siegemund M. The Effect of Albumin Administration in Critically Ill Patients: A Retrospective Single-Center Analysis. Crit Care Med. 2024 May 1;52(5):e234-e244.
14. Callum J, Skubas NJ, International Collaboration for Transfusion Medicine Guidelines Intravenous Albumin Guideline Group. Use of Intravenous Albumin: A Guideline From the International Collaboration for Transfusion Medicine Guidelines. Chest. 2024 Aug;166(2):321-338.
15. Giancarlo et al (2009). Recommendations for the use of albumin. Blood Transfus 2009; 7: 216-34
16. Abedi F, Zarei B, Elyasi S. Albumin: a comprehensive review and practical guideline for clinical use. Eur J Clin Pharmacol. 2024 Apr 12.
17. Joannidis, M., Wiedermann, C.J. & Ostermann, M. Ten myths about albumin. Intensive Care Med (2022).
18. Forster CM, Halls S, Allarakhia S, Modi D, Chung W, Derry K, Digby G, Flemming J, McGugan J, Mackulin H, Montague S, Sibley S, Silver SA, Sirosky-Yanyk A, Stevens A, de Wit K, Zhang L, Callum J. Improving appropriate use of intravenous albumin: results of a single-centre audit and multifaceted intervention. BMJ Open Qual. 2024 Apr 15;13(2):e002534.
ThS.DS.Nguyễn Thiên Vũ
DSCKI. Huỳnh Ngọc Hoàn Mỹ
Đơn vị Dược lâm sàng-thông tin thuốc, Khoa Dược